-
0
سبد خرید
محصول تعداد 0 (ریال)جمع کل

ویژگیهای باتری-ظرفیت
ویژگیهای باتری-ظرفیت
ویژگیهای باتری-ظرفیت
ویژگیهای باتری-ظرفیت یکی از مهمترین ویژگیهای باتری، ظرفیت آن است و بدون ذکر این پارامتر، باتری را درست معرفی نکردهایم. در حقیقت این پارامتر، بیانگر میزان بار موجود در یک باتری است که این باتری میتواند در اختیار ما قرار دهد. هر چه ظرفیت یک باتری بیشتر باشد، مدت زمان دشارژ آن نیز بیشتر است. برای مثال اگر از باتری با ظرفیت بالا در یک وسیلهی پرنده مانند کوادکوپتر استفاده کنیم، این کوادکوپتر، مدت زمان بیشتری را در هوا میماند در حالی که ظرفیت کم، باعث میشود که این وسیلهی پروازی، زودتر خالی شده و به نیاز به شارژ دوباره پیدا کند.
پس تا اینجا فهمیدیم که ظرفیت یک باتری، میزان باریست که در اختیار ما قرار میدهد و همچنین میدانیم که این بار ذخیره شده، قرار است از باتری خارج شده و خود را به صورت جریان نشان دهد. در واقع جریان، آهنگ خروج بارهای الکتریکی از باتریست که در مقالهی قبل، به آن اشاره شد. پس اگر ظرفیت یک باتری بیشتر باشد، معنای آن این نیست که آن باتری جریانش بیشتر است.
واحد ظرفیت، Ah (آمپرساعت) است که همان مقدار کولنی (کولن: واحد بار الکتریکی) است که از باتری خارج میشود و اگر فرض کنیم که جریان یک باتری ثابت باشد، مقدار بار خارج شده از آن برابر با حاصل ضرب جریان در مدت زمان استفاده از باتری است که مطابق فرمول زیر است.
(q(C) = I(A) * ∆t(S
در این فرمول، Q همان ظرفیت باتری است و I جریان آن و ∆t نیز مدت زمان استفاده از آن میباشد که اگر دقت شود، واحد آن ثانیه است در حالی که در بالا ذکر شد که واحد ظرفیت، آمپرساعت است که میتوان با تقسیم این مقدار بر 3600، واحد آمپر ساعت را به دست آورد.
با دقت به واحد ظرفیت، میتوان تعبیر دیگری نیز برای ظرفیت به دست آورد. فرض کنید که ظرفیت یک باتری، 1.8Ah باشد، این عدد میتواند این معنی را داشته باشد که اگر از باتری، به مدت 1 ساعت جریان 1.8 آمپر کشیده شود، این باتری خالی میشود. پس اگر به دنبال آن هستید که باتری شما دیرتر خالی گردد، به دنبال باتری با ظرفیت بالاتر باشید. واحد دیگری که برای ظرفیت استفاده میشود، mAh(میلی آمپرساعت) است که با ضرب عدد 1000 در فرمول قبل، به دست میآید. مثلا 1.8Ah، برابر با 1800mAh است.
معمولا در تجارت باتری، واحد mAh از دیگر واحدها، پرکاربردتر است اما در تحقیقاتی که برای ارتقاء تکنولوژی باتریها انجام میشود، از ظرفیت جرمی و حجمی استفاده میگردد که این مقدار، از تقسیم کردن ظرفیت اولیه، بر جرم یا حجم باتری به دست میآید. اهمیت چگالی ظرفیت، به مراتب از خود ظرفیت بالاتر است زیرا یک باتری را میتوان آن قدر بزرگ ساخت که بار بسیاری درون خود ذخیره کند و در جایگاه مقایسه، مجبوریم که جرمهای(حجمهای) یکسانی را از دو باتری، داشته باشیم تا ببینیم که کدام باتری، ظرفیتش بیشتر است.
مقالات تحقیقاتی، به بررسی چگالی ظرفیت میپردازند و سعی دارند که علاوه بر کاهش جرم باتری، ظرفیت آن را افزایش دهند زیرا با این کار، از جرم نهایی باتری، میکاهیم و میدانیم که جرم باتری، چالش بسیار بزرگ امروز صنعتگران است و اگر جرم باتری کاهش یابد، بسیاری از مشکلات ما نیز حل میشود برای مثال، در خودروهای الکتریکی، مسئلهی وزن، بسیار حائز اهمیت است و با کاهش جرم باتریها، خدمت بسیار بزرگی را به صنعت خودروهای الکتریکی کردهایم.
تا اینجا اهمیت چگالی جرمی و چگالی حجمی ظرفیت را فهمیدیم. فرمول زیر، این دو پارامتر را نشان میدهد که با تقسیم کردن جرم و حجم باتری، این مقادیر به دست میآیند. در عمل، ظرفیت باتری طی گذشت زمان کاهش میابد زیر هر چه که از عمر یک باتری بگذرد، الکترودهای آن باتری فرسوده تر شده و باری که قرار است در اختیار ما بگذارد، کاهش مییابد به همین دلیل است که بعد از گذشت چند سال، باتریهای موبایل، سریعتر خالی شده و ظرفیت اولیه را نخواهند داشت
Q(Ah/g)=q/M Q(Ah/m3)=q/V
حال که با کلیات ظرفیت آشنا شدیم، موقع آن است که کمی بیشتر به این ویژگی بپردازیم. یک باتری از اجزای مختلفی تشکیل میشود که الکترودها، مهمترین قسمتهای آن به حساب میآید. اگر یادمان باشد، ظرفیت را میزان باری که باتری در اختیار ما قرار میدهد، تعریف کردیم پس برای یک الکترود جداگانه نیز میتوان ظرفیت مشخص کرد.
در حقیقت، با تعریف ظرفیت برای یک ماده، ظرفیت باتری شکل میگیرد و میتوان چنین گفت که ظرفیت یک ماده، مقدار باری است که آن ماده در اختیار ما قرار میدهد، و همان طور که اشاره شد، باید جرم آن را نیز لحاظ کرد تا بتوانیم مواد را از لحاظ ظرفیت با یکدیگر مقایسه کنیم. پس ظرفیت مواد، قبل از ظرفیت باتری(پک کامل از الکترودها، الکترولیت و بدنه) تعریف میشود. موقع آن است که کمی حرفهای خود را علمیتر بیان کنیم و با استفاده از فرمولهای ریاضی، مقصود خود را برسانیم.
قبل از همه چیز، خوب است که یک مقدار ثابت را تعریف کنیم که این ثابت، در محاسبات الکتروشیمی، بسیار پرکاربرد است، و آن ثابت فارادی است که آن را با F نمایش میدهیم و معنای آن بار یک مول الکترون است که واحد آن، C/mol (کولن بر مول) میباشد. همان طور که در بالا اشاره گردید، کولن، واحد اندازه گیری بار است که برابر با حاصل ضرب جریان در زمان است و با جایگزین کردن این عبارت به جای کولن، خواهیم داشت:
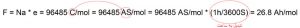
در این رابطه، Na عدد آووگادرو، e بار الکترون، و F نیز ثابت فارادی است که مقدار آن برابر با 26.8A h/mol است. حال که این ثابت را تعریف کردیم، به سراغ محاسبهی ظرفیت جرمی یک ماده میرویم.
برای محاسبهی ظرفیت جرمی یک ماده، از همان تعریف ظرفیت شروع میکنیم و اگر مادهی مورد بررسی، در هنگام اکسایش(یا کاهش)، به تعداد n الکترون آزاد کند، میتوان ادعا کرد که یک مول از این ماده، n مول الکترون آزاد کرده و اگر این مقدار را بر جرم مولی تقسیم کنیم، تعداد مول الکترون بر واحد جرم ماده به دست میآید و برای تبدیل واحد مول به آمپرساعت، کافیست که ثابت فارادی را در آن ضرب کنیم که با این کار، میزان بار الکترون بر واحد جرم به دست میآید که همان ظرفیت جرمی مواد است. معادلات زیر، به راحتی روند محاسبات را نشان میدهد:
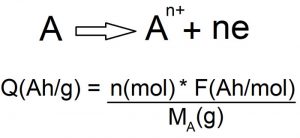
به عنوان مثال، ظرفیت فلز روی را میتوان به همین شکل حساب کرد. فلز روی با جرم مولی 65.4g/mol، و آزاد کردن دو مول الکترون به ازای یک مول از خودش، ظرفیتی برابر با 0.819Ah/g را دارا میباشد که میتوان این عدد را به صورت 819mAh/g نیز بیان کرد. همچنین PbO2 نیز ظرفیتی برابر با 0.224Ah/g را دارد که همانند قبل، میتوان محاسبات خود را انجام داد به این صورت که n، برابر با دو میباشد و جرم مولی آن نیز برابر با 207.2+16*2 =239.2 است.
در جدول زیر، تعدادی از موادی که در آند و کاتد باتریها به کار میرود، آمده است و نکتهی جالب برای این جدول، ظرفیت بالای گازها است که به خاطر جرم سبک آنها این ظرفیت به دست آمده و شاید به همین دلیل است که امروزه تحقیقات بسیار گستردهای برای باتریها بر پایهی گازها انجام میگیرد و به اعتقاد بسیاری از دانشمندان، نسل بعدی باتری، باتریهای بر پایهی گاز است که برای نمونه، میتوان باتریهای لیتیم اکسیژن را برای این نسل، نام برد که امروزه امیدها را برای یک باتری با ظرفیت بالا، زنده نگه داشته است.
از دیگر نکات مهم این جدول، ظرفیت فلز لیتیم است و میبینیم که این فلز، به خاطر سبک بودن، ظرفیت بالایی دارد که این ظرفیت بالا، صنعتگران را وادار به تحقیقات بر روی این فلز کرده است تا بتوانند بدون مشکل، از این فلز در آند باتریهای لیتیم یون استفاده کنند زیرا استفاده از این فلز، مشکلاتی به همراه داشته و باتریهای لیتیم یون بر پایهی این فلز را با محدودیت مواجه کرده که در مقالات آتی، بیشتر به این فلز میپردازیم.
همان طورکه میبینیم، کاتدها، نسبت به آندها، مقدار ظرفیت کمتری دارند و معمولا، محدودیت در کاتد، موجب شده که به فکر مواد جایگزین برای کاتد باشیم و همان طور که اشاره شد، اکسیژن، مادهی بسیار خوبی برای کاتد باتریهاست و همچنین تحقیقات بسیاری را به خود اختصاص داده است. علاوه براکسیژن، سولفور نیز نمایندهی بسیار خوبی برای کاتد است که در این زمینه، در مقالات بعدی، بیشتر صحبت میشود. جدول زیر مقایسه مواد از لحاظ ظرفیت و دیگر پارامترها را نشان میدهد.
|
نوع االکترود |
ظرفیت(Ah/g) |
تعداد الکترون اشتراکیn |
پتانسیل(V) |
جرم مولی(g/mol) |
ماده |
|
آند |
26.59 |
2 |
0 |
2.01 |
H2 |
|
آند |
3.86 |
1 |
3.01- |
6.94 |
Li |
|
آند |
1.16 |
1 |
2.71- |
23.0 |
Na |
|
آند |
2.2 |
2 |
2.38- |
24.3 |
Mg |
|
آند |
2.98 |
3 |
1.66- |
26.9 |
Al |
|
آند |
0.82 |
2 |
0.76- |
65.4 |
Zn |
|
آند |
0.37 |
1 |
2.8- |
72.06 |
LiC6 |
|
آند |
0.26 |
2 |
0.13- |
207.2 |
Pb |
|
کاتد |
3.35 |
4 |
1.23+ |
32.0 |
O2 |
|
کاتد |
0.756 |
2 |
1.36+ |
71.0 |
Cl2 |
|
کاتد |
0.308 |
1 |
1.28+ |
86.9 |
MnO2 |
|
کاتد |
0.432 |
2 |
0.57+ |
123.8 |
AgO |
|
کاتد |
0.224 |
2 |
1.69+ |
239.2 |
PbO2 |
|
کاتد |
0.247 |
2 |
0.01+ |
216.6 |
HgO |
|
کاتد |
0.27 |
1 |
0.14+ |
99.0 |
CuCl |
|
کاتد |
0.231 |
2 |
0.35+ |
231.7 |
Ag2O |
تا الآن فهمیدیم که برای محاسبهی ظرفیت هر ماده، کافیست که با ضرب تعداد الکترون اشتراکی در ضریب فارادی و در نهایت تقسیم آن بر جرم مولی، ظرفیت را حساب کنیم. به دلیل این که در این فرمول، جرم در مخرج قرار دارد، هر چه جرم مولی ماده، کمتر باشد، مقدار ظرفیت افزایش میابد و مطابق جدول بالا، عناصر سنگین نیز، ظرفیت پایین دارند که ناشی از جرم بالای آنهاست.
حال که نحوهی محاسبهی ظرفیت را فهمیدیم، خوب است که ظرفیت یک باتری را که از آند و کاتد تشکیل شده است، محاسبه کنیم. میدانیم که ظرفیت، تعداد الکترونهایی است که در اختیار ما قرار میگیرد و اگر قرار باشد تعداد الکترون یک سمت، از سمت دیگر بیشتر باشد، الکترونهای اضافی، در ظرفیت شرکت نمیکنند زیرا مثلا اگر این الکترونهای اضافی در سمت آند ایجاد شوند، در سمت کاتد، به دلیل این که مادهای وجود ندارد که این الکترونها را دریافت کند(چون ماده در سمت کاتد، به طور کامل مصرف شده است)، جریان باتری صفر شده و دیگر الکترون اضافی تولید نمیشود.
به عبارت بهتر، جرم زیاد یک سمت، بیهوده درون الکترود قرار گرفته است و فقط جرم باتری را افزایش میدهد. پس برای بهینه شدن وزن باتری، باید جرمهای متناسب از هر ماده، درون هر الکترود قرار گیرد و با دشارژ کامل باتری، هر دو الکترود نیز مواد فعال خود را به طور کامل مصرف کنند زیرا این مواد اضافی در واکنش شرکت نمیکنند و فقط وزن باتری و هزینه را افزایش میدهند.
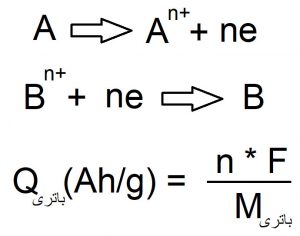
در فرمول بالا جرم باتری، شامل جرم آند، جرم کاتد، جرم الکترولیت، جرم بدنه و سایر اجزای باتری است پس انتظار داریم که ظرفیت تئوری یک باتری، از ظرفیت عملی آن، بسیار بیشتر باشد زیرا در ظرفیت تئوری، هیچ جرمی از اجزای بدنه و دیگر متعلقات آن محاسبه نمیشود. در ظرفیت تئوری یک باتری، ما فقط جرم مواد درگیر واکنش را در نظر میگیریم و اجزای دیگر مانند بدنه و الکترولیت را صرف نظر میکنیم. بدین ترتیب ظرفیت تئوری باتری به شکل زیر محاسبه میشود. دقت شود که در این حالت، مواد مورد استفاده در آند و کاتد، به صورت متناسب استفاده میشود و هیچ مقداری از این دو ماده به صورت اضافه نمیماند
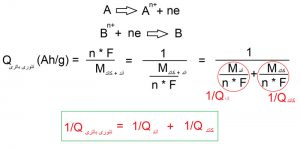
مشاهده میکنیم که برای به دست آوردن ظرفیت تئوری یک باتری، ابتدا ظرفیت آند و کاتد را معکوس کرده و سپس با یک دیگر جمع میکنیم و در نهایت، مقدار حاصله را دوباره معکوس میکنیم تا ظرفیت تئوری به دست آید.
حال وقت آن است که ظرفیت عملی باتریهای تجاری را با یکدیگر ببینیم تا دریابیم که فاصلهی مقادیر تئوری و عملی یک باتری به چه میزان است. جدول زیر، مقادیر عملی ظرفیتها را برای تعدادی از باتریهای موجود در بازار را نشان میدهد.
|
ظرفیت جرمی(Ah/g) |
جرم(g) |
ظرفیت(Ah) |
نام باتری |
|
0.052 |
50 |
2.6 |
Panasonic/Sanyo |
|
0.058 |
48 |
2.8 |
Samsung ICR18650-28A |
|
0.066 |
30 |
2.0 |
Tenergy NiMH |
|
0.022 |
18 |
0.4 |
Combo LiFePO4 |
ملاحظه میکنیم که این مقادیر بسیار از مقادیر تئوری مواد فاصله دارند ودلیل آن نیز بالا رفتن جرم باتری به دلیل اضافه شدن جرم بدنه و جرم جمعکنندهی جریان(Current Collector) است و باعث شده که در عمل، ظرفیت به شدت افت کند.
خلاصه و نتیجه گیری:
در این مقاله به ویژگی دیگر باتری یعنی ظرفیت پرداختیم و گفتیم که ظرفیت به صورت مقدار باری که یک باتری میتواند در اختیار ما قرار دهد، تعریف میشود. در ادامه به محاسبهی ظرفیت یک ماده پرداختیم و با بیان فرمولها، منظور خود را بهتر انتقال دادیم.
در نهایت، با تعریف مقدار تئوری ظرفیت یک باتری، فرمول سادهای برای آن ارائه کردیم و شرط استفاده از این فرمول را نیز، متناسب بودن مقدار ماده در دو سمت باتری دانستیم و دلیل آن را نیز، عدم استفاده از جرم اضافه در باتری بیان کردیم و گفتیم که اگر جرمهای مواد فعال در آند و کاتد متناسب نباشد، وزن باتری بدون افزایش در ظرفیت، زیاد میشود و یک مقدار بیهوده از مواد فعال را در باتری استفاده کردیم و فقط جرم و هزینهی باتری را بالا بردهایم بدون آنکه ظرفیت افزایش یابد.
پس تناسب جرم در دو سمت، بسیار اهمیت دارد. در این مقاله، به ظرفیت حجمی یک باتری نیز اشاره شد که برای پرهیز از گفتن مطالب تکراری، از شرح و بسط آن صرفه نظر شد ولی به صورت کلی، تمام حرفهایی که برای ظرفیت جرمی گفته شد، برای ظرفت حجمی نیز صادق است با این تفاوت که به جای جرم باتری، حجم باتری مورد نظر است و در تمام فرمولها، به جای جرم، از حجم استفاده میشود.
- برچسب:
- باتری خودرویی
- باتری صنعتی
- باتری لیفتراکی
- باتری مخابراتی
- باتری اسیدی
- باتری برق اضطراری
- باتری سیلد ساکن
- باتری UPS
- باتری یو پی اس
- باتری قلیایی
- باتری لیتیوم یونی
- صبا باتری
- اتمی
- باتری خشک
- باتری اسید سربی
- باتری معدنی
- باتری قلمی لیتیومی